引言:地方时9月29日,美国食品药品安全管理处批准了由Amylyx制药公司研发的药物Relyvrio可以治疗肌肉萎缩多发性硬化症成年人病人。该药物是第一款在任意、安慰剂对照临床研究中明显减缓ALS肿瘤进展并且能够增加存活文章正文引言:本地
引言:
地方时9月29日,美国食品药品安全管理处批准了由Amylyx制药公司研发的药物Relyvrio可以治疗肌肉萎缩多发性硬化症成年人病人。该药物是第一款在任意、安慰剂对照临床研究中明显减缓ALS肿瘤进展并且能够增加存活
文章正文引言:
地方时9月29日,美国食品药品安全管理处批准了由Amylyx制药公司研发的药物Relyvrio可以治疗肌肉萎缩多发性硬化症成年人病人。该药物是第一款在任意、安慰剂对照临床研究中明显减缓ALS肿瘤进展并且能够增加存活期的治疗方法药物,都是116年至今FDA批准第3款ALS医治药物。这一款疗法获准全过程可以说一波三折。除此之外,下一个ALS新药很有可能马上就会来临,在今年的7月渤健和Ionis制药公司的在研反义寡核苷酸治疗法上市申请已获FDA审理,并赋予其优先审评资质,核查新药的最后期限定为2023年1月25日。期待更多渐冻症自主创新治疗法产品研发成功,尽早赶到病人身旁。
渐冻症新药美国获准到底是怎么一回事,和小编一起看看吧。
(人民日报健康手机客户端 陈艳辉)地方时9月29日,美国食品药品安全管理处(FDA)批准了由Amylyx制药公司研发的药物Relyvrio(苯丁酸钠和赖氨酸二醇内服固定不动使用量秘方,AMX0035)可以治疗肌肉萎缩多发性硬化症(ALS,别名“渐冻症”)成年人病人。该药物是第一款在任意、安慰剂对照临床研究中明显减缓ALS肿瘤进展并且能够增加存活期的治疗方法药物,都是116年至今FDA批准第3款ALS医治药物。
这一款疗法获准全过程可以说一波三折。在今年的3月,FDA咨询委员会以6:4的投票结果,表明临床试验数据尚不兼容这一款治疗法实效性。以后,Amylyx公司提交了对临床数据的进一步剖析及其来源于其他临床研究的大力支持数据信息,并第一次得到澳大利亚监管部门的批准如果有条件发售。
在今年的6月,FDA通告Amylyx制药公司,将核查新药的最后期限延至9月29日,便于有更多的时间核查苯丁酸钠和赖氨酸二醇内服固定不动使用量秘方(AMX0035)临床实验数据库的附加剖析。
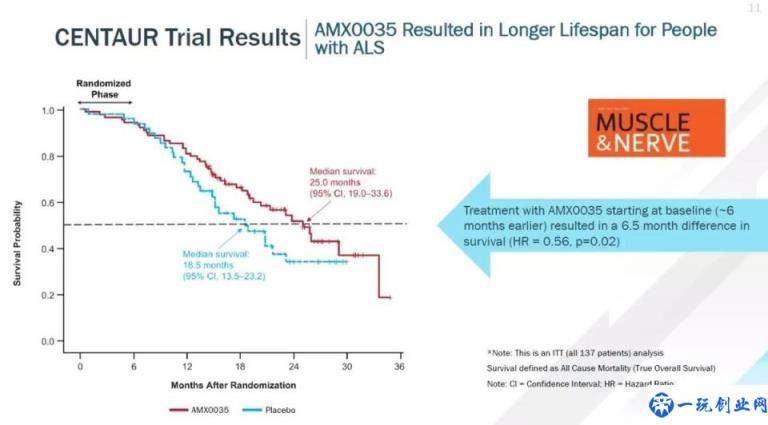
9月8日,FDA外围和中枢系统药物咨询委员会(PCNSDAC)以7:2的投票结果赞同Amylyx制药公司在研药物AMX0035的目前实验数据足够适用其可以治疗肌肉萎缩侧索硬化的上市申请。现阶段苯丁酸钠和赖氨酸二醇内服固定不动使用量秘方(AMX0035)在ALS患者中的三期临床试验正在进行,方案于2023年底或2024年初进行。

据ALS协会官网详细介绍,ALS协会曾将2014年ALS冰桶挑战赛筹取的220万美金投向这类药物的开发,还领导干部了将近数十年的宣传策划健身运动,以便这一治疗法得到批准,包含在2020年9月向FDA递交了超出5万只签字,号召FDA批准该药物。
肌肉萎缩多发性硬化症(ALS)是上运动神经元和下运动神经元损害以后,致使包含球部(所说球部,是指延髓支配的这一部分肌肉组织)、四肢、躯体、乳房腹部的肌肉组织慢慢乏力和委缩。此病一般进度快速,过半数病人确诊均值预期寿命为3-5年,最终多丧生于吸气肌肉无力所导致的心力衰竭。
除此之外,下一个ALS新药很有可能马上就会来临,在今年的7月渤健和Ionis制药公司的在研反义寡核苷酸治疗法上市申请已获FDA审理,并赋予其优先审评资质,核查新药的最后期限定为2023年1月25日。期待更多渐冻症自主创新治疗法产品研发成功,尽早赶到病人身旁。
渐冻症新药美国获准延伸阅读:
美国食品药物管理处批准医治“渐冻症”新药物
地方时9月29日,美国食品药物管理处(FDA)批准了由Amylyx制药公司研发的药物Relyvrio,将作为一种医治肌肉萎缩多发性硬化症 (ALS,别名“渐冻症”)的新的方法。
(由来:CCTV新闻app)
精彩不断新闻资讯请于应用商店下载“极目新闻”手机客户端,未授权切勿转截,诚邀给予新闻信息,一经采取即刷酬劳。24钟头报料热线027-86777777。
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至 举报,一经查实,本站将立刻删除。


